Синдром Гийена — Барре: особенности редкой неврологической патологии

Фото из открытых источников носит иллюстративный характер.
Синдром Гийена — Барре: особенности редкой неврологической патологии
Синдром Гийена — Барре недавно оказался на слуху благодаря новости о таком диагнозе у бывшего российского политического деятеля Анатолия Чубайса, который на отдыхе в Италии попал в реанимацию с «отнявшимися ногами и руками, перекошенным лицом». Довольно редкое острое аутоиммунное заболевание в период пандемии стало встречаться чаще, поскольку основным триггером его развития являются перенесенные незадолго до этого инфекции (вирусные и бактериальные), в том числе коронавирусная инфекция, вызванная SARS-CоV-2.
О клинической симптоматике, основных аспектах дифференциальной диагностики, методах лечения синдрома Гийена — Барре в интервью «Медвестнику» рассказал доцент кафедры неврологии и нейрохирургии БелМАПО, кандидат мед. наук Михаил Селицкий.
Что представляет собой синдром Гийена — Барре?

Михаил Селицкий, доцент кафедры неврологии и нейрохирургии БелМАПО, кандидат мед. наук
Это патологическое состояние, при котором иммунная система человека начинает поражать собственные периферические нервы. Включает в себя несколько клинических форм. Чаще всего это острая воспалительная демиелинизирующая полиневропатия — ОВДП. В этой аббревиатуре отражены основные аспекты: заболевание начинается остро или подостро, имеет воспалительный характер, но не является инфекционным, поражает миелиновую оболочку периферических нервов и вызывает неврологические нарушения.
Миелиновая оболочка, окутывающая периферические нервы, выполняет множество функций, важнейшая из них — ускорение проведения импульса по периферическому нерву. Соответственно клиническая симптоматика связана с замедлением проведения нервных импульсов. В случае типичной формы, ОВДП, поражаются в первую очередь моторные нервы, страдает функция иннервируемых ими мышц, нарушается моторика, развиваются парезы.
Отличительный признак синдрома Гийена — Барре — симметричность, то есть страдают обе ноги, затем обе руки (парапарез, тетрапарез). Хотя встречаются и казуистические случаи с несимметричным дебютом. При атипичных формах поражается не только миелиновая оболочка, но и осевые цилиндры — аксоны периферических нервов, что часто приводит к более длительному течению и восстановлению пациента. Таких форм две — острая моторная аксональная невропатия (ОМАН) и острая моторно-сенсорная аксональная невропатия (ОМСАН). Еще одна атипичная форма синдрома Гийена — Барре — пандизавтономия, когда страдают исключительно вегетативные волокна периферических нервов, иннервирующих внутренние органы — сердце, легкие, кишечник, тонус сосудов, потоотделение.
Наиболее редкая разновидность среди атипичных форм — синдром Миллера — Фишера, он встречается в 2–3 % случаев. Для данного синдрома характерно быстрое (в течение нескольких дней) развитие глазодвигательных нарушений (офтальмоплегии), нарушение координации движений (атаксии) и арефлексии.
Что является причиной этого острого неврологического заболевания?
Этиология синдрома Гийена — Барре неизвестна. А вот триггеры, пусковые факторы достаточно неплохо изучены. К ним относятся различные инфекции — респираторные, желудочно-кишечные и другие, в том числе коронавирусная инфекция, вызванная SARS-CoV-2. Инфекция ломает иммунитет, который начинает вырабатывать антитела к миелину собственных нервных клеток. Пусковыми факторами синдрома Гийена — Барре также могут быть другие события, активирующие иммунную систему, например, травма, хирургическое вмешательство. В международных публикациях описаны случаи синдрома Гийена — Барре после вакцинации, в том числе некоторыми вакцинами против коронавирусной инфекции. Поэтому нужно быть осторожными, внимательными к себе и своим близким и при появлении неврологических симптомов сразу обращаться за медицинской помощью.
В подавляющем большинстве случаев у пациента в анамнезе за 1–2 недели до развития неврологических симптомов отмечается то или иное инфекционное заболевание, даже совсем легко перенесенное (небольшое покашливание, диарея, кратковременное повышение температуры).
Как развивается клиническая симптоматика?
При типичном варианте синдрома Гийена — Барре (острой воспалительной демиелинизирующей полиневропатии) симптомы начинаются с дискомфорта в нижних конечностях, который затем постепенно, но быстро — в течение часов или дней — переходит на руки. Например, утром пациент жалуется на онемение и слабость в ногах, к вечеру или на следующий день появляется слабость в руках. В отсутствие адекватного лечения при прогрессировании заболевания возможно поражение черепных нервов, которые иннервируют органы и ткани головы. В процесс вовлекается черепная мускулатура, у пациента перекошено лицо, могут не закрываться глаза и т. д. Но наиболее опасный вариант — поражение 10-й пары черепных нервов с нарушением работы дыхательной и сердечно-сосудистой систем. Такое состояние носит название синдрома Ландри, и в основном с ним связана летальность при синдроме Гийена — Барре. Опасность синдрома Ландри в стремительном прогрессировании: от вовлечения в процесс черепной мускулатуры до полной остановки дыхания может пройти менее суток или вовсе часы.
Какие сложности встречаются в процессе диагностики синдрома Гийена — Барре, особенно в амбулаторно-поликлиническом звене, куда, как правило, в первую очередь обращается пациент?
Действительно, на первых этапах, когда пациента смотрит врач общей практики в поликлинике или фельдшер скорой, им непросто сразу распознать тонкую неврологическую симптоматику синдрома Гийена — Барре. Легче диагностировать, когда заболевание имеет типичную клиническую картину — постепенное симметричное поражение конечностей. Однако встречаются, хоть и редко, фокальные формы, когда слабеет только одна рука и/или одна нога. Врач, в том числе невролог, увидев гемипарез, в первую очередь заподозрит инсульт. Даже у нас в 5-й ГКБ Минска, которая является клинической базой кафедры неврологии и нейрохирургии БелМАПО, такие случаи бывают, когда пациент с гемипарезом и нераспознанным синдромом Гийена — Барре госпитализируется в сосудистое отделение для больных с инсультом. Но одностороннее поражение при инсульте так и остается односторонним (за исключением быстрого повторного инсульта), с постепенным регрессом или стабилизацией. А при нераспознанном синдроме Гийена — Барре ассиметричное начало быстро переходит на вторую сторону, клиническая картина становится более развернутой, и диагноз уже не вызывает сомнений. Пациент переводится в общее неврологическое отделение и получает патогенетическое лечение.
Диагностические ошибки на амбулаторно-поликлиническом этапе возникают также при дебюте заболевания, когда на первый план выходят не моторные, а сенсорные нарушения. Пациент приходит в поликлинику, жалуется на боли в спине в грудном или поясничном отделе, с иррадиацией в конечности. То есть описывает корешковые боли, как при радикулите. В итоге диагноз ошибочно выставляется по болевому синдрому: радикулит, вертеброгенная торакалгия, миофасциальный болевой синдром и пр. Присоединение моторной симптоматики — а при синдроме Гийена — Барре присоединяется практически всегда! — заставляет впоследствии усомниться в первоначальных предположениях и продолжить диагностический поиск.
Наиболее сложная для распознавания форма — острая пандизавтономия. У пациента нет парезов, нет болей, нет сенсорных нарушений, но он перестает держать давление, ему трудно дышать, у него нарушена перистальтика кишечника, появляется сердечная аритмия.
Какие инструментальные и лабораторные методы обследования необходимо выполнить в ходе диагностического поиска при подозрении на синдром Гийена — Барре?
Основным инструментальным методом, с помощью которого мы можем объективизировать нарушение проведения импульса по периферическому нерву, является электронейромиография (ЭНМГ), но она показывает замедление проведения импульса только по моторным и сенсорным волокнам. К сожалению, иногда в первые 7 дней от начала заболевания прибор не распознает нарушений и выдает норму. Если же избирательно страдают вегетативные волокна, например, в случае пандизавтономии, то на ЭНМГ мы также увидим нормальную картину, и это может сбить клинициста с постановки правильного диагноза.
Характерным лабораторным маркером синдрома Гийена — Барре является повышение уровня белка в спинномозговой жидкости при нормальном уровне лейкоцитов, это называется белково-клеточной диссоциацией. Однако данный маркер проявляется только к концу первой недели заболевания, иногда даже к 10–14-му дню. А клиническая симптоматика развивается за 2–3 дня. Поэтому бывает, что пациент поступает с типичной клинической картиной синдрома Гийена — Барре, ему выполняют люмбальную пункцию и при анализе ликвора получают норму, то есть ложноотрицательный результат. ЭНМГ тоже в норме. В итоге врач, видя типичную картину демиелинизирующей полиневропатии, но не находя инструментального и лабораторного подтверждения, начинает новый диагностический поиск. Это в корне неправильный подход. Лично мое мнение: синдром Гийена — Барре — это клинический диагноз. Если он подтверждается ЭНМГ — хорошо, если нет — нельзя исключать синдром Гийена — Барре. Повторив люмбальную пункцию и переделав ЭНМГ через неделю, вы увидите типичные для этого заболевания изменения.
Как не ошибиться при выставлении диагноза по клинической неврологической симптоматике? Особенно на начальном этапе, когда это делает ВОП или фельдшер скорой помощи?
Михаил Селицкий:
В первую очередь следует установить характер пареза: центральный или периферический. Это очень важно для постановки топического диагноза. Так, при поражении головного и спинного мозга развивается центральный парез, а при повреждении корешков, сплетений, периферических нервов — периферический. Симптоматика в этих случаях будет разной. Для центрального пареза характерно повышение мышечного тонуса, наличие патологических рефлексов, повышение сухожильно-периостальных рефлексов. При периферическом — рефлексы снижаются, мышечный тонус низкий, патологических рефлексов нет. Клинически, когда мы видим острый симметричный периферический парез, особенно восходящего характера от ног к рукам, это практически всегда синдром Гийена — Барре. Повторюсь, вне зависимости от инструментальных и лабораторных исследований.
Следует также учитывать, что при острой патологии спинного мозга (любого характера — сосудистого, воспалительного в виде миелита или при травме) в первые несколько суток возможен так называемый спинальный шок. И получается, что пострадала ЦНС, но клинически при осмотре мы видим периферический нижний парапарез. Однако для спинальной симптоматики характерны другой тип нарушения чувствительности, нарушение функций тазовых органов, отсутствие постепенного восходящего нарастания пареза. Неврологическая картина развивается сразу ниже уровня поражения спинного мозга. Знание этих клинических особенностей позволяет с высокой вероятностью заподозрить или по крайней мере не исключить синдром Гийена — Барре даже при ложноотрицательных результатах.
Как проходит лечение синдрома Гийена — Барре?
Поскольку непосредственная причина поломки иммунитета неизвестна, то этиологического лечения не существует. Но достаточно хорошо изучен патогенез, доказан аутоиммунный характер патологических процессов, поэтому основными методами лечения являются иммуносупрессия и иммуномодуляция. Цель — убрать антитела, разрушающие миелин. Есть два способа. Первый — плазмаферез, то есть чистка крови, вымывание и удаление патологических антител. Второй — введение внутривенных иммуноглобулинов, дорогостоящий, но эффективный метод. Внутривенные иммуноглобулины меняют работу иммунитета таким образом, что патологические антитела перестают вырабатываться и заболевание останавливается. Миелин постепенно начинает восстанавливаться и, как следствие, уходит симптоматика заболевания.
Мы в 5-й ГКБ применяем два метода. Их эффективность примерно одинакова как по международным данным, так и по нашему собственному опыту. Но по каждому методу есть те или иные противопоказания. Поэтому определяем лечение с учетом индивидуальных особенностей, сопутствующих заболеваний, существующих противопоказаний.
Сколько длится лечение, какое количество сеансов плазмафереза необходимо? Каковы дозировки и схема введения внутривенного иммуноглобулина?
Считается, что при плазмаферезе должно промыться 30–50 мл крови на кг массы тела. Число сеансов определяет врач-трансфузиолог, но в среднем получается от 2 до 5 сеансов. После каждого берутся анализы, чтобы не пропустить осложнения, поскольку вымываются не только патологические аутоантитела, но и белки, многие другие полезные молекулы. Если все нормально, что на 3–4-е сутки проводится повторный сеанс. Обычно 2 раза в неделю, иногда 3. Таким образом, на весь курс плазмафереза нужно 1–2 недели.
При введении внутривенных иммуноглобулинов применяем стандартную международную схему: 0,4 г на кг в сутки в течение 5 дней. Суммарная доза получается 2 г на кг. Пациент взвешивается, рассчитывается количество лекарства, которое ему нужно, и в течение 5 дней равными дозами каждый день в виде обычных капельниц пациент получает лечение.
Помимо патогенетического лечения назначается также симптоматическая терапия. Она не влияет на механизм заболевания, но уменьшает симптоматику. Назначаем обезболивающие (при жалобах пациента на боль), антихолинэстеразные препараты для улучшения проведения импульсов по нервам, сосудистые средства, чтобы улучшить микроциркуляцию в тканях и тем самым уменьшить воспаление. Витамины группы В способствуют регенерации, также липоевая кислота и др.
Каков прогноз после перенесенного синдрома Гийена — Барре? Как проходит восстановление нарушенных функций? Необходима ли реабилитация?
Прогноз в большинстве случаев благоприятный, летальность при синдроме Гийена — Барре составляет около 2–3 %. Самое главное — своевременно назначить патогенетическую терапию, тогда даже очень тяжелые в неврологическом плане пациенты хорошо восстанавливаются. Причем клиническое восстановление подтверждается инструментально. На контрольных осмотрах (через полгода, год) повторяем ЭНМГ и отмечаем улучшение электрофизиологических показателей вплоть до полной нормализации.
Скорость восстановления разная. Некоторые пациенты в течение месяца восстанавливаются полностью, реабилитация им не нужна. Рекомендуем избегать респираторных заболеваний, соблюдать нормальный режим труда и отдыха, полноценный сон, сбалансированное питание. Но чаще восстановление пострадавших функций идет медленно, нужна реабилитация: лечебная физкультура, механотерапия, иглорефлексотерапия, повторные курсы физио-, симптоматической терапии. Пациента нужно всегда предупреждать, чтобы он не пугался, если через 2 месяца, например, у него ноги слабые. Главное, что процесс восстановления начался и он постепенно, но идет. В некоторых случаях может потребоваться 2–3 месяца, полгода, год, а по некоторым публикациям и 2 года. Остаточные нарушения после 2 лет, как правило, уже необратимы, и с ними придется жить. Патогенетическое лечение назначается однократно.
К слову, синдром Гийена — Барре редко рецидивирует, лишь в казуистических случаях может повториться дважды в течение жизни. Но сейчас у нас в стационаре есть пациент, у которого в течение года повторно остро развилась классическая симптоматика синдрома Гийена — Барре. В первый раз после лечения он полностью восстановился, сейчас получаеттерапию внутривенными иммуноглобулинами и также неплохо восстанавливается.
Отличается ли синдром Гийена — Барре после перенесенного COVID-19 от спровоцированного другими инфекциями?
Наша кафедра неврологии и нейрохирургии БелМАПО сейчас занимается научно-исследовательской работой, финансируемой Минздравом и посвященной неврологическим осложнениям при COVID-19. Изучаем в том числе полиневропатии, не только острые, как синдром Гийена — Барре, но и хронические. После подтвержденного COVID-19 встречаются как типичный синдром Гийена — Барре, так и его атипичные формы. Проанализировав статистические данные, увидели, что в сравнении с доковидным периодом стало больше атипичных аксональных форм — ОМАН и ОМСАН, которые протекают сложнее и тяжелее классической. Почему так, пока трудно сказать. Набираем данные, анализируем корреляцию клинической, электрофизиологической картины, иммунологического статуса и т. д. Но факт, что СOVID-19 может провоцировать синдром Гийена — Барре, не вызывает сомнений.
Много таких пациентов? Зависит ли тяжесть развившегося синдрома Гийена — Баре от тяжести перенесенной коронавирусной инфекции?
Михаил Селицкий:
За весь период пандемии в нашей больнице пролечено более 20 пациентов с синдромом Гийена — Барре, ассоциированным с COVID-19. А в целом в нашей базе более 40 таких пациентов, которые обращались на кафедру из других учреждений Минска, регионов республики за консультациями. В основном это пациенты старше 35–40 лет. По нашим наблюдениям, степень тяжести синдрома Гийена — Барре не коррелирует с тяжелым течением COVID-19. Встречаются пациенты, которые очень тяжело перенесли коронавирусную инфекцию, с пневмонией, респираторной поддержкой, но в классическом легком варианте переносят синдром Гийена — Барре. И наоборот, в анамнезе за неделю кратковременное недомогание с небольшим повышением температуры, подтвержденный ПЦР-тестом COVID-19, кажущееся выздоровление, а через 2–3 дня тяжелейший синдром Гийена — Барре с быстрым развитием синдрома Ландри.
Хотелось бы подчеркнуть для врачей-реаниматологов: если синдром Гийена — Барре имеет быстрый восходящий характер, с распространением на черепные нервы и риском развития синдрома Ландри, очень важно, чтобы пациент был переведен в реанимационное отделение. Даже если на момент осмотра реаниматологом у пациента нормальное давление, он хорошо дышит, все равно он должен быть переведен в реанимацию.
В таких случаях на фоне кажущегося благополучия может внезапно развиться остановка сердца и дыхания и потребоваться немедленное подключение к ИВЛ, а это проблематично при нахождении пациента в обычном отделении. И если не успеть подключить к ИВЛ за несколько минут, то потенциально благоприятный прогноз перечеркнется летальностью. Алгоритм прост: при вовлечении черепных нервов и риске синдрома Ландри пациент обязательно должен находиться в реанимации 2–3 дня. Назначили патогенетическое лечение, увидели стабилизацию — переводите обратно в соматическое отделение.
Зарубежный опыт СГБ на фоне пандемии: есть ли связь с COVID-19?

На прошедшем недавно республиканском семинаре «Междисциплинарные возможности взаимодействия при нервно-мышечных заболеваниях у взрослых» обсуждался в том числе и синдром Гийена — Барре. С докладом выступил Мариуш Семинский, профессор Гданьского медицинского университета (Польша). Предлагаем вашему вниманию некоторые затронутые в докладе нюансы.
Заболевание встречается относительно редко, Меньше всего в Японии — 0,44 на 100 тысяч человек в год. В Европе и Северной Америке ежегодно 2–2,3 на 100 тысяч населения.
В Южной Америке в последнее время наблюдалось больше случаев из-за эпидемии вируса Зика.
Характерным для синдрома Гийена — Барре является тот факт, что до появления неврологической симптоматики пациент переносит какую-либо инфекцию, такая связь обнаруживается примерно у 60 %. Мариуш Семинский также акцентировал внимание на других факторах риска. В частности, условиями, повышающими вероятность синдрома Гийена — Барре, являются все виды иммуноопосредованных заболеваний, а также ревматологические заболевания, трансфузии. У женщин к факторам риска относится преэклампсия.
В странах Юго-Восточной Азии прослеживается связь синдрома Гийена — Барре с инфекцией Campylobacter jejuni, она выявляется примерно в 1/3 случаев. В Европе синдром Гийена — Барре чаще связан с цитомегаловирусной инфекцией или вирусом Эпштейна — Барр. У 1/3 пациентов предшествующая специфическая инфекция не выявляется.
— Кроме того, синдром Гийена — Барре может быть связан с вакцинацией, — сообщил профессор. — Хотя распространено мнение, что чем больше людей вакцинировано, тем меньше вероятность вирусных и бактериальных инфекций, и вакцинация таким образом приводит к уменьшению частоты синдрома Гийена — Барре.
В странах Западной Европы наиболее распространенной является острая воспалительная демиелинизирующая полиневропатия, при которой ключевым элементом патологического процесса служит повреждение миелина. Клинически она в большинстве случаев проявляется прогрессирующей слабостью нижних и верхних конечностей. В странах Азии преобладают аксональные повреждения с острой моторной и/или сенсорной нейропатией.
Одна из актуальных тем — специфическая связь COVID-19 и синдрома Гийена — Барре.
— Опубликовано множество отдельных статей и обзоров, но все, что нам известно сегодня, это факт, что COVID-19, как и любая другая инфекция, может спровоцировать синдром Гийена — Барре, — подчеркнул Мариуш Семинский. — Но разве это особая форма синдрома? Похоже, совсем нет. Как и при типичном синдроме Гийена — Барре, симптоматика появляется через несколько недель после инфицирования SARS-CoV-2 и в большинстве случаев представляет классическую форму с тетрапарезом. В Европе наиболее распространенной формой СГБ после COVID-19 является острая воспалительная демиелинизирующая полиневропатия.
Профессор привел данные испанских исследователей: из 400 тысяч пациентов, обратившихся в отделение неотложной помощи, было выявлено более 70 тысяч человек с COVID-19, среди них 11 случаев синдрома Гийена — Барре, что составило примерно 0,15 на 1 000 — в 7 раз выше, чем у пациентов без COVID-19.
Мариуш Семинский:
По данным других стран, такой значительной разницы не прослеживается. В национальном обсервационном исследовании в Великобритании показано отсутствие прямой связи между более высокой заболеваемостью COVID-19 и числом случаев синдрома Гийена — Барре. Интересная ситуация в Сингапуре, там на фоне пандемии, наоборот, отмечено резкое снижение случаев данного синдрома. Лечение СГБ, спровоцированного SARS-CoV-2, традиционное: обменный плазмаферез и внутривенные иммуноглобулины. Большинство опубликованных на данный момент случаев основаны на успешном лечении внутривенным иммуноглобулином. Хорошо задокументированных случаев с применением плазмафереза не так много.
По мнению Мариуша Семинского, такая разная картина в странах обусловлена простым фактом: увеличение числа случаев синдрома Гийена — Барре, ассоциированного с COVID-19, компенсируется снижением таких случаев, спровоцированных другими инфекциями (респираторными и ЖКТ) благодаря ограничительным мерам при пандемии (социальное дистанцирование, требования гигиены, ношение масок).
Хроническая воспалительная демиелинизирующая полиневропатия с острым началом у беременной

Владимир Пономарев, заведующий кафедрой неврологии и нейрохирургии БелМАПО, доктор мед. наук, профессорХроническая воспалительная демиелинизирующая полиневропатия (ХВДП) — одна из самых частых форм аутоиммунных полиневропатий, для которой характерно преимущественное поражение корешков и периферических нервов конечностей. Распространенность ХВДП в Беларуси составляет 2,1 случая на 100 тысяч населения. Ранняя диагностика имеет важное значение, учитывая тот факт, что заболевание является потенциально курабельным, течение и исход во многом зависят от сроков начала патогенетической терапии. В свою очередь несвоевременное лечение ХВДП сопровождается вторичной аксонопатией, что приводит к тяжелым резидуальным явлениям, ухудшению трудоспособности и качества жизни.
Критерии диагностики
В настоящее время наиболее достоверными международными критериями диагностики ХВДП являются критерии, разработанные Европейской федерацией неврологических сообществ (EFNS) в 2010 году. Основополагающим методом выступает стимуляционная электронейромиография (ЭНМГ) в сочетании с клинической картиной.
Клинические критерии ХВДП представлены в табл. 1.
Типичные ЭНМГ-признаки заболевания включают снижение скорости проведения импульса (СПИ), увеличение дистальной латентности и временной дисперсии, блоки проведения, увеличение латентности F-волны.
ХВДП и синдром Гийена — Барре

Михаил Селицкий, доцент кафедры неврологии и нейрохирургии БелМАПО, кандидат мед. наукНаиболее схожим с ХВДП заболеванием, по клинической картине и данным ЭНМГ, считается синдром Гийена — Барре (СГБ). Основной разграничительной чертой является только длительность прогрессирования неврологических симптомов. Для типичной формы ХВДП свойственно развитие симптоматики не менее 8 недель от начала заболевания, а для синдрома Гийена — Барре — не более 4 недель.
Рядом авторов выделены другие отличительные черты иммунопатогенеза ХВДП и СГБ. В частности, различия клеточного и гуморального звеньев иммунитета в их патогенезе. Так, при ХВДП отмечается снижение числа клеток с фенотипом CD8+ и количества натуральных киллеров, что может способствовать развитию и/или прогрессированию аутоиммунного процесса. Кроме того, у пациентов с ХВДП выявлено значимое снижение уровней иммуноглобулинов классов IgG и IgA. В свою очередь у пациентов с СГБ констатировано снижение клеток CD4+ и повышение содержания иммуноглобулинов класса IgM.
В современной литературе описаны случаи типичного клинического течения ХВДП, которая начиналась достаточно остро. Нозологическая принадлежность и подходы к терапии в таких случаях дискутируются. Большинство авторов рассматривают их как атипичную форму заболевания, которая названа ХВДП с острым началом (оХВДП), ее частота может достигать 16 % всех случаев ХВДП. С другой стороны, СГБ может протекать с рецидивами или иметь волнообразное изменение клинической картины на протяжении всего лечения, что сближает его с ХВДП.
Вопрос дифференциальной диагностики оХВДП и синдрома Гийена — Барре обсуждается научным международным сообществом. В 2015 году японские авторы попытались выявить клинические особенности, сравнив две группы пациентов. Результаты работы показали, что пациенты с оХВДП имели более выраженные сенсорные нарушения, а развитие вегетативной, дыхательной недостаточности, нарушение функции лицевого нерва, предшествующее инфекционное заболевание были менее значимыми. Различий в ЭНМГ-показателях не было выявлено. Российскими авторами, напротив, описан случай ХВДП с острым началом и дыхательной недостаточностью. При этом авторы сообщают о значительных трудностях в дифференциальной диагностике и лечении молодой пациентки, которой первоначально был ошибочно выставлен диагноз СГБ.
Большинство авторов сходятся во мнении, что на ранней стадии заболевания невозможно определенно сказать, с каким именно диагнозом невролог столкнулся — СГБ или оХВДП, и лишь тщательный мониторинг клинической картины и сроков прогрессирования заболевания позволяет дифференцировать эти нозологические формы.
Полиневропатии и беременность
Немаловажную роль в развитии, течении и прогнозе любого аутоиммунного заболевания играет беременность. Вероятно, влияние беременности на течение любого аутоиммунного заболевания вызвано изменением гормонального фона в организме женщины и, как следствие, нарушением иммунных реакций организма.
В литературе встречаются единичные случаи сочетания ХВДП и беременности. В 1987 году впервые описан дебют ХВДП на фоне беременности. В 1992 году группой авторов описан случай спонтанного регресса симптоматики сразу после родов у пациентки с ХВДП. Также в литературе имеются данные о случае ХВДП, когда после прерывания беременности наблюдалась длительная ремиссия заболевания. Случаев развития оХВДП на фоне беременности в доступных источниках нами не обнаружено.
Лечение: воздействие на патогенез и симптоматику
ХВДП и СГБ имеют во многом схожие подходы к патогенетическому лечению. К ним относится назначение плазмафереза и внутривенных иммуноглобулинов (ВВИГ). Глюкокортикостероиды (ГКС) являются препаратами первой линии только при ХВДП, в то время как назначение их при СГБ является врачебной ошибкой. Учитывая невозможность дифференциального диагноза ранних стадий СГБ и ХВДП, сопоставимый лечебный эффект плазмафереза и ВВИГ, менее выраженные побочные реакции у ВВИГ, наиболее предпочтительным методом лечения является использование последних в общепринятой курсовой дозе 2 г/кг. Известно, что после однократного курса ВВИГ не всегда удается достичь полного восстановления или длительной ремиссии ХВДП, поэтому актуальным остается вопрос изучения лечебного эффекта при повторных курсах человеческого нормального иммуноглобулина G.
Изучаются аспекты длительности назначения и кратности приема не только ВВИГ, но и подкожных иммуноглобулинов (ПКИГ). Показана эффективность ПКИГ при таких заболеваниях, как миастения гравис и мультифокальная моторная невропатия. Метаанализ, опубликованный в 2016 году, продемонстрировал, что ВВИГ и ПКИГ обладают равным эффектом при ХВДП и мультифокальной моторной невропатии (ММН), но использование ПКИГ связано с лучшей переносимостью. В этой связи ПКИГ можно рассматривать как альтернативу ГКС при длительном лечении пациентов с ХВДП.
Таблица 1. Клинические диагностические критерии ХВДП (EFNS/PNS, 2010).

Клинический случай. Пациентка В., 28 лет, в сроке 20 недель беременности обратилась за медицинской помощью с жалобами на слабость и онемение в конечностях. Вышеописанные жалобы появились 2 дня назад утром, без видимой причины. Первым симптомом было онемение в стопах, затем в течение суток присоединилась слабость в ногах, потом в руках и незначительный прозопарез с двух сторон. Госпитализирована в отделение анестезиологии и реанимации акушерско-гинекологической службы 6-й ГКБ Минска с подозрением на инсульт. В тот же день после консультации дежурного невролога с предположительным диагнозом «синдром Гийена — Барре» переведена для дальнейшего лечения в реанимационное отделение роддома 5-й ГКБ Минска.
Диагноз при поступлении: острая воспалительная демиелинизирующая полиневропатия (ОВДП), прогрессирующее течение, с преимущественно проксимальным тетрапарезом (выраженным в руках, умеренным в ногах), легкой diplegia facialis.
Анамнез жизни: из перенесенных заболеваний — простудные, ветряная оспа, хронический гастрит, эрозия шейки матки. Наследственный и аллергологический анамнезы не отягощены. В акушерско-гинекологическом анамнезе: три беременности, из них двое родов в срок и один выкидыш.
Соматический статус при поступлении полностью компенсирован: АД 120/70 мм рт. ст., пульс 64 уд/мин, частота дыхания 15 в минуту, температура тела и сатурация (SpO2) в пределах нормы.
Неврологический статус при поступлении: легкая слабость мимических мышц с двух сторон, периферический тетрапарез (в руках проксимально — 2 балла, дистально — 4 балла; в ногах проксимально — 3 балла, дистально — 4 балла), сухожильно-периостальные рефлексы (СПР) с ног не вызывались, с рук — были снижены, равновелики. Патологических стопных знаков не было. Отмечалось нарушение поверхностной чувствительности на стопах по типу «носков». Мышечно-суставное чувство не нарушено. Умеренная болезненность нервных стволов при пальпации. Менингеальные симптомы отрицательные.
Обследования с целью дифференциальной диагностики (указаны только лабораторные показатели, отклоняющиеся от нормальных). ОАК: гемоглобин 104 г/л, СОЭ 62 мм/ч; ОАМ: белок — 0,055 г/л, бактерии ++; БАК: альбумин 31,45 г/л, креатинин 45,86 мкмоль/л, мочевина 1,98 ммоль/л, лактатдегидрогеназа 283 Ед/л, С-реактивный белок 33,08 мг/л; коагулограмма — все показатели в норме; анализы крови на сифилис и ВИЧ — отрицательные; анализ цереброспинальной жидкости (на 6-е сутки заболевания): белок 0,63 г/л, цитоз 4/3; ПЦР крови к ДНК цитомегаловируса положительная, к вирусу простого герпеса и вирусу Эпштейна — Барр отрицательная; анализ крови на антитела (IgM) к ЦМВ — не обнаружено.
УЗИ органов брюшной полости: спленомегалия, умеренная двусторонняя нефромегалия, диффузные изменения паренхимы почек с признаками умеренного отека. Эхокардиография: клинически значимых изменений нет. Рентгенография органов грудной клетки: без патологии.
ЭКГ: ритм синусовый, нормальное положение электрической оси сердца, признаки гипертрофии левого желудочка. МРТ шейного и поясничного отделов позвоночника: признаки дегенеративно-дистрофических изменений; МРТ головного мозга: патологических объемных образований не выявлено, МР-картина умеренной смешанной гидроцефалии.
ЭНМГ: признаки первично-демиелинизирующего поражения моторных и сенсорных волокон нервов верхних и нижних конечностей (см. рис. 1 и 2). ЭНМГ-показатели в динамике приведены в табл. 2.
Консультация уролога: гестационный пиелонефрит. Консультация инфекциониста: острая ЦМВ-инфекция, осложненная ОВДП. Противовирусное лечение не показано.
Течение заболевания. В первый день поступления пациентки в 5-ю ГКБ (третьи сутки заболевания) начат курс ВВИГ в дозе 0,4 г/кг № 6. Несмотря на это, наблюдалось прогрессирование двигательных нарушений до выраженного тетрапареза, усугубился прозопарез до умеренного справа, развились дисфагия, дисфония, дизартрия.
На 9-е сутки заболевания у пациентки произошел самопроизвольный выкидыш. Назначен подкожный иммуноглобулин (гамманорм) в дозе 0,15 г/кг ежедневно (7 дней). Кроме этого проводилась антибактериальная, инфузионная, симптоматическая терапия (витамины В1, В6, В12, С, антиоксиданты, ингибиторы ацетилхолинэстеразы, антикоагулянты), физиотерапевтическое лечение, лечебная физкультура.
На фоне проводимого лечения к 15-му дню заболевания прекратился восходящий тип прогрессирования неврологических симптомов. С 20-го по 60-й дни заболевания у пациентки наблюдалось постепенное восстановление функции черепных нервов, в то время как степень тетрапареза, преимущественно дистального, продолжала прогрессировать. К 60-м суткам у пациентки отмечались: легкая слабость мимических мышц с двух сторон, периферический тетрапарез (в руках проксимально 4 балла, дистально 1 балл; в ногах проксимально 4 балла, дистально 0 баллов); бульбарные нарушения и нарушения чувствительности на лице регрессировали. Гипотрофии мышц кистей и стоп, СПР с рук и ног не вызывались. Патологических стопных знаков не было. Отмечалось нарушение поверхностной чувствительности в виде гиперестезии с гиперпатией на кистях и стопах. Грубое нарушение мышечно-суставного чувства и вибрационной чувствительности на стопах. Болезненность нервных стволов при пальпации.
Дальнейшая тактика
Учитывая прогрессирование симптомов свыше 8 недель, согласно международным критериям диагностики, пациентке клинический диагноз был изменен на ХВДП с острым началом и назначен ПКИГ (гамманорм) в дозе 0,4 г/кг еженедельно. На 70-е сутки заболевания пациентка вновь забеременела, но при этом лечение гамманормом было ей продолжено в прежней дозировке. Спустя 5 месяцев от начала заболевания двигательные и чувствительные нарушения восстановились практически полностью, оставалась только минимальная слабость разгибателей стоп. Введение гамманорма прекращено на 145-е сутки заболевания, и спустя еще 20 дней у пациентки случился повторный самопроизвольный выкидыш. К 6-му месяцу болезни все неврологические симптомы регрессировали полностью.
Полученные результаты и обсуждение
Представленный клинический случай характеризуется рядом особенностей. Вероятно, провоцирующими факторами развития заболевания являлись беременность и цитомегаловирусная инфекция (верифицированная с помощью ПЦР). Данный случай является исключением из клинической практики, так как, согласно мировым данным, установить провоцирующий фактор удается только в 20 % случаев ХВДП.
Типичная нарастающая (восходящая) клиническая картина в начале заболевания привела к постановке диагноза ОВДП, и только непрерывный мониторинг за состоянием пациентки позволил выставить правильный диагноз ХВДП.
Особенностью клинической картины являлось длительное (свыше 8 недель) прогрессирование тетрапареза, вплоть до плегии в стопах, на фоне восстановления функций черепных нервов. Проведенный в динамике контроль ЭНМГ-данных показал, что на фоне уже восстановившихся двигательных функций (6-й месяц заболевания) имело место выраженное структурное повреждение периферических нервов, что подтверждалось данными ЭНМГ.
Трудным был вопрос выбора патогенетической терапии, т. к. в Беларуси нет утвержденных протоколов лечения беременных пациенток, страдающих ОВДП или ХВДП. Опираясь на данные международных авторов и собственный опыт, было принято решение о назначении ВВИГ, имеющих, по данным литературы, наименьшие побочные эффекты при беременности среди других известных методов патогенетического лечения.
Впервые была пролечена ПКИГ (гамманорм) беременная пациентка, страдающая атипичной формой ХВДП с острым началом. Более того, это был первый опыт непрерывного длительного (более трех месяцев) лечения иммуноглобулинами с использованием комбинации форм внутривенного и подкожного введения.
Учитывая, что стабилизация и постепенное улучшение симптомов заболевания совпали с началом повторной беременности и назначением длительного курса гамманорма, нельзя исключить иммуносупрессивный эффект непосредственно самой беременности. Уникальность данного случая заключается в том, что заболевание протекало на фоне двух беременностей, которые закончились самопроизвольными абортами и, вероятно, сыграли немаловажную роль в течении самого заболевания.
Рисунок 1.

Рисунок 2.
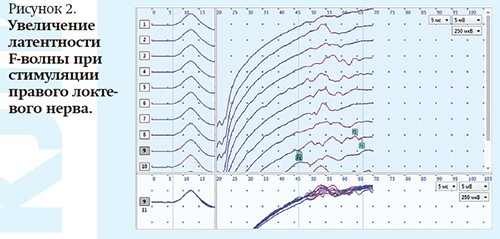
Таблица 2. ЭНМГ-показатели в динамике.

Источник: medvestnik.by
Комментарии закрыты.